
科学精准防控风险 着力提升监管效能——辽宁、山东、云南三省药监局合力打造重点品种智慧监管新模式
为强化药品全生命周期信息化管理,深入推进药品智慧监管场景应用,在国家药监局信息中心指导下,辽宁、山东、云南三省药监局协同开展药品生产数字化监管示范项目建设,以“科学精准防控风险,着力提升监管效能”为核心目标,针对疫苗、特殊药品、血液制品、中药注射剂等重点品种,依托信息化系统建设,探索基于风险的重点品种智慧监管策略,并形成可复制、可推广的普适性成果。
一、明确主题思路 锚定建设目标
按照国家药监局信息中心的统筹部署,辽宁、山东、云南三省药监局统一思想,共同商定项目建设目标、建设思路、实施路径、计划方案,加强协调联动,合力推进项目建设,充分发挥示范项目的引领作用,打造药品智慧监管新模式。通过示范项目建设,督促药品上市许可持有人全面提升药品生产全过程的信息化管理,提高药品全生命周期管理水平,推动生物医药产业转型升级,深化推进工业互联网创新发展。通过实施智慧监管,以技术创新和应用创新推动药品生产监管模式创新,推动传统监管模式向“在线智控”、“精准监管”转变,通过实时远程监管和动态风险预警,提升风险预警和应急处置能力,真正“让监管跑在风险前面”。
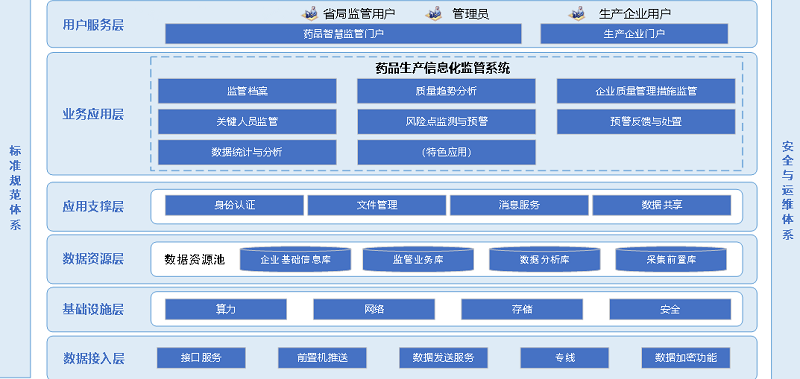
图1 药品生产数字化监管项目总体架构
二、明确责任分工 强化机制保障
辽宁、山东、云南三省药监局按照“锚定总体目标思路—分工协作个别建设—总结归纳提纯提质”的工作思路,成立专班强化组织,定期调度增进互动,充分发挥各自优势,分享经验解决困难,有力保障实施进度,共同推进示范项目建设,形成加强重点品种监管业务协同、合力探索药品智慧监管模式的良好局面。在示范项目建设的过程中,三省药监局共同构建起了全流程数据标准体系、安全的数据交互方案、智能的风险预警模型、完善的风险闭环体系,围绕运用信息技术为监管赋能的主旨思想,强化监管实践与信息技术的深度融合,保障示范项目顺利实施。
三、明确建设路径 注重应用实效
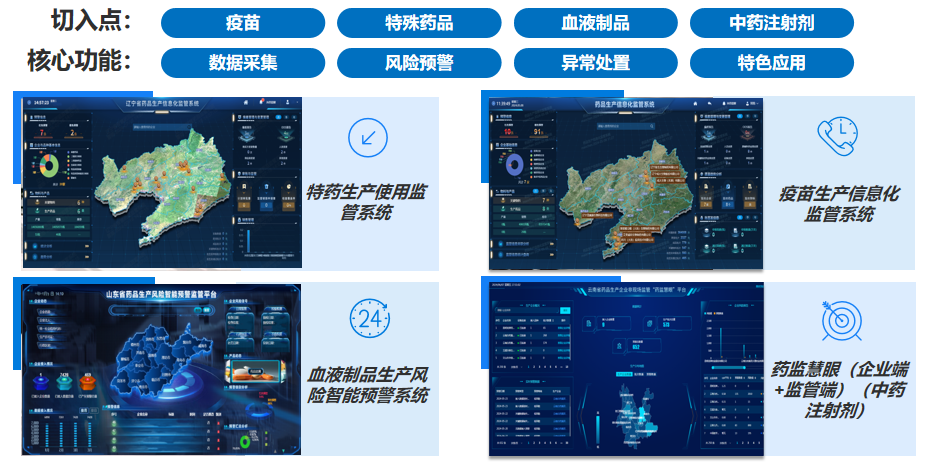
辽宁、山东、云南三省药监局始终以“科学精准防控风险,着力提升监管效能”为核心,围绕疫苗、特殊药品、血液制品、中药注射剂等重点品种的特定风险确定监管需求,将药品法律法规要求和监管实践经验提炼、转化为数字化的关键参数和逻辑算法,基于风险防控要素和重点监管部位建立关键质量数据集。通过对数据进行实时分析和智能比对,实现构建企业画像、动态过程监控、异常趋势分析、风险监测预警、辅助现场检查等应用场景,破解了潜在隐患及时感知、重大风险即时防控的监管难题,并在一定程度上解决了监管人员能力差异化的问题。同时,在示范项目的建设当中,突出数据安全管理。基于“六横三纵”的架构建设监管系统,通过设置前置机、数据加密、专线传输、身份认证、政务云部署等一系列数据安全策略,保障数据交互、数据存储等全过程的安全防护。
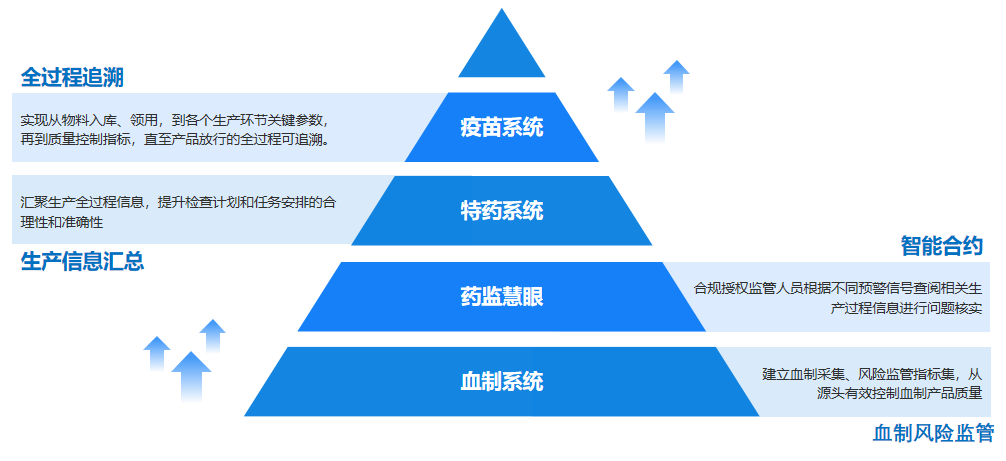
四、明确示范成果 注重应用实效
辽宁、山东、云南三省药监局在示范项目的推进过程中,注重经验总结和成果转化,形成了一系列具有借鉴和推广价值的制度文件和技术标准。例如,在药品生产信息化监管领域的建设标准方面,建立了《药品生产智慧监管技术方案》《药品生产信息化监管系统建设标准》《药品生产企业数据采集技术方案》《疫苗生产信息化监管系统建设技术方案》《特殊药品生产使用信息化监管系统建设技术方案》《药品生产风险智能预警系统(血液制品)建设方案》等技术标准;在探索跨地域、跨部门协调联动、协同监管方面,辽宁省药监局制定了《辽宁省药品监督管理局关于全面启动实施疫苗生产信息化监管系统的通知》《辽宁省疫苗生产信息化监管系统使用管理规定(暂行)》,与辽宁省工信厅联合研究制定关于生物医药产业数字化转型升级的实施意见;云南省药监局制定了《云南省药品监督管理局关于加快推进“药监慧眼”工程实施的通知》《云南省生物医药产业数据资源共享协议》等文件。
在示范项目建设过程中,形成的经验成果除了在三省药监局之间得以借鉴推广,同时还有其他5个省级药监局进行了实地调研。辽宁省疫苗生产信息化监管系统还在2024年全国药品监督管理工作会议及“天坛药政沙龙——数字化转型关键路径与方法交流会”上作交流发言,并作为药品监管部门唯一参展项目在第七届数字中国建设峰会上展出。
五、示范带动全局 推进全面实施
各省级药监局将在国家药监局信息中心的统一指导下,以重点品种数字化监管示范项目为起点,全面推进信息技术与药品监管的深度融合,深化数据利用和监管赋能,增进药品智慧监管的广度和深度,开拓新领域,丰富新维度,完善新机制,探索新模式,推动药品智慧监管迭代升级和持续发展,不断提升药品监管能力的现代化水平。



 京公网安备 11010202010537号
京公网安备 11010202010537号 